Gugus Fungsi Senyawa Hidrokarbon Materi Kimia Kelas 12 – Kimiawan terdahulu, menyebut senyawa yang ada di hewan dan tumbuhan dengan senyawa organik. Setelah diteliti, ditemukan bahwa semua senyawa organic yang ada di alam, memiliki kesamaan yakni mengandung unsur karbon dan hidrogen. secara umum senyawa yang mengandung unsur karbon dan hidrogen disebut dengan senyawa hidrokarbon.
Perhatikan senyawa hidrokarbon berikut:
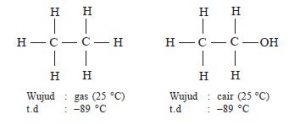
Kedua senyawa diatas memiliki jumlah unsur Karbon ( C) dan Hidrogen (H) yang sama, namun memiliki sifat yang sangat berbeda. Hal ini disebabkan karena satu atom -H pada gambar pertama digantikan dengan gugus –OH pada gambar kedua. Hal inilah yang menyebabkan terjadinya perbedaan yang signifikan pada senyawa karbon diatas.
-OH adalah salah satu gugus fungsi. Gugus Fungsi adalah atom atau gugus atom yang menjadi ciri khas suatu senyawa dimana hal ini menentukan struktur dan sifat suatu senyawa. Senyawa dengan gugus fungsi sama biasanya mempunyai karakteristik yang mirip sehingga disatukan pada golongan yang sama.
1. Pengertian Gugus Fungsi
Gugus fungsi adalah kelompok atom dalam suatu senyawa organik yang menentukan sifat kimia senyawa tersebut. Kehadiran gugus fungsi memberikan reaktivitas tertentu pada molekul hidrokarbon.
2. Jenis Gugus Fungsi pada Senyawa Hidrokarbon
a. Alkohol (-OH)
- Struktur Umum: R-OH
- Contoh: Etanol (C₂H₅OH)
- Sifat: Larut dalam air, sifat polar, dapat membentuk ikatan hidrogen.
b. Alkohol Primer, Sekunder, dan Tersier
- Berdasarkan posisi gugus -OH pada atom karbon:
- Primer: Terikat pada karbon yang hanya berikatan dengan satu gugus alkil.
- Sekunder: Terikat pada karbon dengan dua gugus alkil.
- Tersier: Terikat pada karbon dengan tiga gugus alkil.
c. Aldehida (-CHO)
- Struktur Umum: R-CHO
- Contoh: Formaldehida (HCHO), Asetaldehida (CH₃CHO)
- Sifat: Berbau khas, sifat reaktif, digunakan dalam pelarut dan resin.
d. Keton (-C=O)
- Struktur Umum: R-CO-R’
- Contoh: Aseton (CH₃COCH₃)
- Sifat: Non-polar, pelarut organik yang baik.
e. Asam Karboksilat (-COOH)
- Struktur Umum: R-COOH
- Contoh: Asam asetat (CH₃COOH), Asam benzoat (C₆H₅COOH)
- Sifat: Bersifat asam, larut dalam air, menghasilkan ion H⁺ di larutan.
f. Ester (-COO-)
- Struktur Umum: R-COO-R’
- Contoh: Metil asetat (CH₃COOCH₃)
- Sifat: Wangi khas, digunakan pada parfum dan flavoring.
g. Eter (R-O-R’)
- Struktur Umum: R-O-R’
- Contoh: Dietil eter (C₂H₅OC₂H₅)
- Sifat: Tidak reaktif, digunakan sebagai pelarut.
h. Amina (-NH₂, -NHR, -NR₂)
- Struktur Umum: R-NH₂
- Contoh: Metilamina (CH₃NH₂)
- Sifat: Bersifat basa, digunakan dalam pembuatan plastik dan obat-obatan.
i. Amida (-CONH₂)
- Struktur Umum: R-CONH₂
- Contoh: Urea (CO(NH₂)₂)
- Sifat: Larut dalam air, stabil secara kimia.
3. Reaktivitas Gugus Fungsi
Sifat reaktif gugus fungsi menentukan jenis reaksi kimia yang dapat terjadi, seperti:
- Oksidasi: Alkohol → Aldehida/Keton → Asam Karboksilat.
- Hidrolisis: Ester → Asam Karboksilat + Alkohol.
- Reaksi Substitusi: Halogen pada senyawa halida.
4. Pentingnya Gugus Fungsi dalam Kehidupan
- Farmasi: Gugus fungsi menentukan sifat obat.
- Industri: Digunakan untuk membuat plastik, bahan bakar, parfum, dan zat pewarna.
Tabel Gugus Fungsi
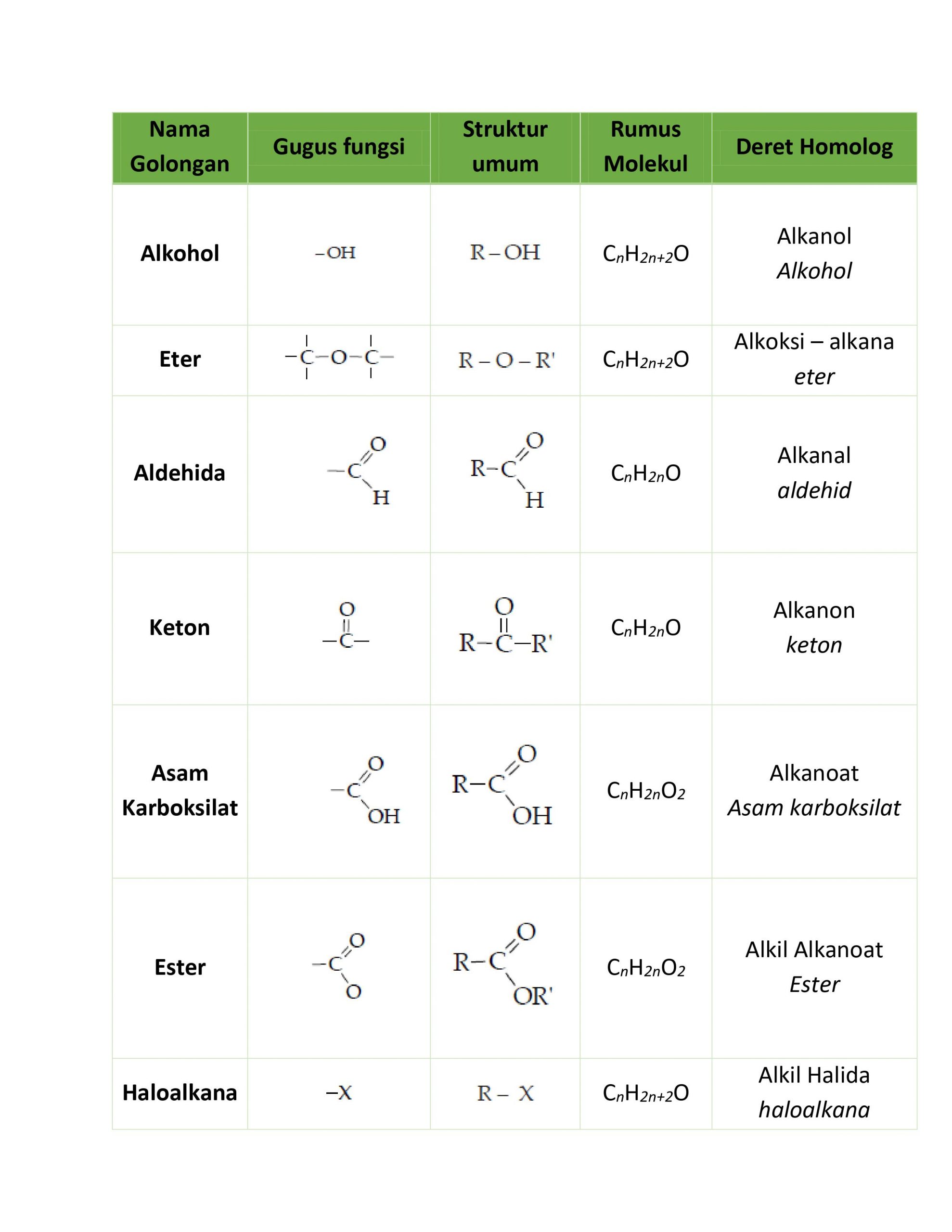
Ket: R = Alkil
Gugus fungsi itulah yang merupakan bagian paling reaktif jika senyawa tersebut bereaksi dengan senyawa lain. Sehingga jika senyawa hidrokarbon ini direaksikan dengan senyawa lain, gugus fungsilah yang akan mengalami perubahan.
Penutup
Gugus fungsi merupakan salah satu topik penting dalam kimia organik yang memengaruhi sifat dan reaktivitas senyawa hidrokarbon. Dengan memahami jenis-jenis gugus fungsi seperti alkohol, aldehida, keton, asam karboksilat, dan lainnya, kita dapat menganalisis berbagai reaksi kimia dan aplikasinya dalam kehidupan sehari-hari, mulai dari bidang farmasi hingga industri. Pemahaman ini juga menjadi dasar penting untuk mendalami materi kimia organik di tingkat lanjutan.
FAQ
1. Apa itu gugus fungsi?
Gugus fungsi adalah kumpulan atom dalam molekul yang menentukan sifat kimia dan reaktivitas dari senyawa tersebut.
2. Mengapa gugus fungsi penting dipelajari?
Gugus fungsi membantu kita memahami sifat kimia senyawa, pola reaksi, dan aplikasinya dalam berbagai bidang seperti farmasi, makanan, dan industri.
3. Apa perbedaan antara alkohol primer, sekunder, dan tersier?
- Primer: Gugus -OH terikat pada karbon yang hanya berikatan dengan satu gugus alkil.
- Sekunder: Gugus -OH terikat pada karbon yang berikatan dengan dua gugus alkil.
- Tersier: Gugus -OH terikat pada karbon yang berikatan dengan tiga gugus alkil.
4. Apa contoh senyawa yang memiliki gugus fungsi karbonil (-C=O)?
- Aldehida: Formaldehida (HCHO).
- Keton: Aseton (CH₃COCH₃).
5. Apa yang dimaksud dengan reaksi oksidasi pada alkohol?
Reaksi oksidasi pada alkohol adalah proses di mana alkohol diubah menjadi aldehida, keton, atau asam karboksilat tergantung pada kondisi reaksinya.
6. Bagaimana cara membedakan senyawa aldehida dan keton?
- Aldehida memiliki gugus karbonil (-C=O) di ujung rantai karbon.
- Keton memiliki gugus karbonil (-C=O) di tengah rantai karbon.
7. Apa manfaat senyawa dengan gugus fungsi dalam kehidupan sehari-hari?
Senyawa ini digunakan untuk berbagai keperluan, seperti bahan baku obat-obatan, parfum, plastik, pelarut, dan makanan.
Selamat belajar, semoga bermanfaat!